Для выбора варианта лечения необходима своевременная и достоверная диагностика Н.Рylori.
Все способы диагностики Н.Pylori, используемые в настоящее время, условно можно разделить на прямые и не прямые (косвенные). На инвазивные и неинвазивные [5, 7]. Инвазивные методы требуют проведения биопсии слизистой оболочки желудка при эндоскопическом обследовании, неинвазивное – не требуюет биопсии. Прямые методы позволяют непосредственно выявить H.Pylori. Косвенные методы регистрируют не саму бактерию, а последствия ее персистирования в организме.
Большинство прямых методов, основаны на инвазивных способах забора материала. Прямая диагностика инфекции H.Pylori, является достаточно трудоемким и отсроченным во времени процессом [13].
После принятия Маастрихтского консенсуса [14] несколько лет в странах Европы существовала концепция "тестирования и эндоскопии" ("testing and endoscopy") [15]. Последняя заключалась в том, что при первичном обращении пациента тестировали на наличие инфекции H. Pylori, и при положительных результатах, обязательно проводили эндоскопическое исследование. Однако, опыт повседневной практики показал неоправданное увеличение количества гастроскопий, которое не компенсировалось положительными эффектами в виде улучшения симптоматики или же повышения качества жизни пациентов. Необходимость в проведении гастроскопии при желудочной диспепсии диктуется онконастороженностью врачей. Вместе с тем, известно, что для пациентов молодого возраста при отсутствии тревожных симптомов в виде потери массы тела или анемии в превалирующем большинстве случаев злокачественные новообразования желудка не характерны. Поэтому для первичных пациентов с язвенной болезнью начали использовать как обязательную концепцию "тестировать и лечить" ("test and treat"), принятую на Маастрихтском консенсусе II в 2000 году [10, 16-19]. Руководящие органы здравоохранения многих стран рекомендуют такой же подход для ведения первичных пациентов молодого возраста. Возрастные границы в рекомендациях варьируют в зависимости от уровня заболеваемости раком желудка в конкретной популяции (таблица 1). Возрастной порог составляет 45 - 55 лет [20-26].
Таблица 1. Пороговый возраст при использовании концепции "test and treat"
| Организация | Пороговый возраст, годы |
| Британское гастроэнтерологическое общество | < 55 |
| Европейское общество первичной помощи в гастроэнтерологии | < 45 |
| Европейская группа по исследованию H.Рylori | < 45 |
| Американская гастроэнтерологическая ассоциация | < 45 |
| Руководство Шотландской межуниверситетской сети | < 55 |
В соответствии с выработанной концепцией Маастрихтского консенсуса II, Европейской и Российской группами были приняты диагностические алгоритмы, определяющие проведение первичной диагностики инфекций H.Pylori неинвазивными методами: серологическим, дыхательным, ПЦР в кале и слюне.
В России для быстрой диагностики H.Рylori зарегистрированы серологические тесты на основе латекс-агглютинации и сэндвич-метода: FastRead H.Рylori® (CQI-biomed) и Pyloriset® Dry (Orion Diagnostica). Преимуществом этих методик является простота их выполнения и быстрота получаемого результата. К недостаткам следует отнести невысокую степень чувствительности и специфичности, а также невозможность количественного определения антител к Н.Рylori, что не позволяет их использовать для контроля за эрадикацией.
Среди неинвазивных методов диагностики Н.Рylori, за рубежом наиболее распространен серологический иммуноферментный анализ: в крови пациента определяют антитела IgG, IgM к Н.Рylori [27-32]. Данные тесты оптимальны для эпидемиологических исследований и скрининга. Такие исследования проводятся во всех западных странах. В качестве примера можно привести обследование, проведенное в Италии, с помощью ИФА-тестов 1010 доноров, у 298 из которых были определены антитела IgG к Н.Pylori [23]. При последующей гастроскопии у 70 (23,5%) человек из IgG серопозитивной группы выявлены пептические язвы, у 41 (13,8%) – эрозивный дуоденит, у 2 (0,7%) – рак желудка. К сожалению, в России не проводят аналогичные плановые исследования по выявлению инфицированности населения Н.Pylori, хотя скрининг, направленный на обнаружение антител к Н.Рylori, способствует выявлению лиц с гастродуодеальной патологией. Своевременная диагностика и последующая адекватная терапия помогают предотвратить рецидивы заболевания и исключить инфицированность Н.Рylori больших групп населения.
До последнего времени серологические тесты рассматривали только с позиций выявления Н.Рylori у пациентов до лечения. Действительно, существовали ограничения, затрудняющие проведение мониторинга эффективности эрадикации Н.Рylori с их помощью. Последнее связано с тем, что исходное значение концентрации специфических антител к Н.Рylori в сыворотке крови пациентов, установленное стандартными ИФА-тестами, варьирует в значительных пределах, а снижение ее после эрадикации бактерии имеет нелинейный характер. Современное поколение ИФА-тестов, благодаря усовершенствованию технологии сорбции антигена и модификации данного метода, позволяет количественно оценивать степень инвазии H.Pylori, а также степень эрадикации [33-37]. Различными авторами доказано, что снижение титра специфических антител к Н.Pylori на 40% от исходного позволяет констатировать эрадикацию более чем у 90% больных к 3 месяцу после окончания лечения. Серонегативность у всех вылеченных больных наступает через 12 месяцев [38].
В таблице 2 представлены литературные данные по чувствительности, специфичности, предсказательной ценности положительного результата (РРV) и предсказательной ценности отрицательного результата (NPV) наиболее используемых в мире серологических тестов [39].
Таблица 2. Характеристики серологических тестов для выявления НР
| Наименование тест-системы | Чувствительность,% | Специфичность,% | PPV | NPV |
| Oxoid Unipath, Latex agglutination | 93 | 83 | 87 | 91 |
| Pyloriset dry Orion, Murex latex | 77 | 100 | 100 | 80 |
| GAP IgG ELISA Био-Рад, ИФА | 100 | 84 | 90 | 100 |
| ИммуноКомб Орженикс, ИФА | 98,1 | 86 | 100 | 97 |
| Pyloriset EIA-G Orion, Murex | 93 | 90 | 91 | 92 |
| Helisal OneStep, Cortecs Diagnostics | 84,1 | 63,0 | 73,3 | 76,6 |
Как видно из представленных данных, чувствительность и специфичность ИФА тест-систем выше аналогичных показателей серологических тестов на основе латекс-агглютинации и сэндвич-метода.
При выборе методов диагностики Хеликобактериоза для данной медицинской технологии были учтены следующие факторы:
- чувствительность, специфичность и достоверность тестов;
- возможность количественного определения антител к H.Pylori;
- неравномерное оснащение различных институтов, клиник, стационаров и поликлиник современной диагностической аппаратурой и реактивами;
- необходимость в укреплении диагностической службы первичной медицинской помощи современными высокотехнологичными, доступными методами диагностики.
Из зарегистрированных в Российской Федерации, вышеперечисленным требованиям отвечают иммуноферментные Быстрые Простые Тесты ИммуноКомб H.PILORI IGG (Орженикс), как наиболее чувствительные, специфичные, позволяющие количественно определить титр антител IgG в сыворотке, плазме или цельной крови. БПТ ИммуноКомб не требуют специальной квалификации персонала и дополнительного оборудования. Методика ИммуноКомб основана на оригинальной модификации твёрдофазного иммуноферментного анализа: зубцы пластикового гребня сенсибилизированы соответствующими антигенами или антителами, ячейки ванночек заполнены готовыми растворами конъюгата, промывочными буферами и красителем. При проведении анализа зубцы гребня приводят в контакт с исследуемыми образцами в первом ряду ванночки, а далее последовательно переносят из ячейки в ячейку. В случае положительного результата на зубце гребня появляются точки (окрашенные комплексы антиген-антитело). Правильность постановки анализа подтверждается появлением на зубце контрольного пятна. Учёт результатов – визуальный (для количественной оценки результатов сравнивают интенсивность окраски точек в опыте со стандартной цветовой шкалой, входящей в состав набора) или автоматический с помощью прибора КомбСкан Набор позволяет провести от 1 до 36 анализов, время анализа - 66 минут, срок годности наборов 9 месяцев.
Тест-системы Иммунокомб сертифицированы СЕ 0459 и широко используются более чем в ста странах мира. Тесты ИммуноКомб удовлетворяют всем стандартам качества, установленным директивой 98/79/EC Европейского парламента и Совета для in-vitro диагностики.
Производство тест-систем ИммуноКомб имеет GMP Certificate и соответствует нормам ВОЗ. Качество тестов подтверждено международными стандартами SI ISO 9001:1994, и ISO 13485:1996 и Европейскими стандартами EN 928:2001, EN 928:1996, EN 980:1997, EN 13612:2002, EN 13640:2002, EN 13641:2002, EN 46001:1996
Как достоверные, высокочувствительные и специфичные тесты ИммуноКомб отобраны для программ ВОЗ, Юнеско, Красного Креста. Проверены и одобрены институтом П.Эрлиха (Германия), институтом А.Фурниэ (Франция), AFSSAPS, ГИСКом им. Тарасевича.
В настоящее время БПТ ИммуноКомб комплектуются в России совместным предприятием ЗАО «Биоград» (Санкт-Петербург) из реагентов, производимых фирмой Орженикс.
В 1997 г., в ГИСК им. Л.А.Тарасевича, при проведении Государственных испытаний с целью регистрации Иммуноферментного БПТ ИммуноКомб H.PILORI IGG фирмы Орженикс, был проведен сравнительный анализ предлагаемой методики с референс-ИФА тест-системой фирмы Био-Рад «Иммуноферментный набор для количественного определения антител к Helicobacter Pylori IgG» (Регистрационное удостоверение МЗМПР № 97/316). Сравнение проводилось на 30 человеческих сыворотках от взрослых и детей с патологией пищеварительного тракта и здоровых, либо больных с поражением других органов. Для анализа полученных данных была составлена таблица сопряженности двух признаков: первый признак – выявление IgG антител к H.Pylori в сыворотках по методике Орженикс и второй признак – выявление указанных антител по методике Био-Рад. Четыре сыворотки были отброшены, т.к. не могли быть оценены при помощи референс-метода. Данные представлены в таблице 3 [40].
Таблица 3. Сопряженность выявления антител к H.Pylori двумя методиками
| Био-Рад | Положительные | Отрицательные | Сумма |
| Орженикс | |||
| Положительные | 19 | 2 | 21 |
| Отрицательные | 0 | 5 | 5 |
| Сумма | 19 | 7 | 26 |
l1 = 21, m1 = 19, n = 26
l2 = 5, m2 = 7
Статистическая обработка данных показала относительно большое значение 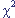 = 16,8, свидетельствующее о том, что признаки сильно сопряжены друг с другом. Отметим также, что коэффициент корреляции в данном случае оказывается равным 0,8 и это также свидетельствует о наличии сильной связи двух рассматриваемых признаков.
= 16,8, свидетельствующее о том, что признаки сильно сопряжены друг с другом. Отметим также, что коэффициент корреляции в данном случае оказывается равным 0,8 и это также свидетельствует о наличии сильной связи двух рассматриваемых признаков.
Таким образом, по данным проведенного эксперимента можно сделать вывод, что сравниваемые методики приблизительно эквивалентны.
Клинические испытания проводились в клинике гастроэнтерологии детской клинической больницы № 7 г. Москвы.
Всего было исследовано 95 сывороток.
В детской больнице была исследована 41 сыворотка от детей с различной гастропатологией и 18 – от здоровых и детей с другими диагнозами, не связанными с нарушениями функций желудочно-кишечного тракта. Параллельно с серологическим методом, основанным на применении диагностического набора ИммуноКомб ИммуноКомб H.PILORI IGG, диагноз у пациентов устанавливали совокупностью методов клинической диагностики: эндоскопическим исследованием, рентгеноскопией и т.д. При сопоставлении данных клинической диагностики и серологического исследования были получены следующие цифры: у детей, страдающих различными формами гастрита, гастродуоденита, язвенной болезнью и полипозом, повышенный уровень IgG антител к H.pylori выявлялся в 24 случаях, что составляло 58,5%. При обследовании взрослых пациентов (всего в группе 36 больных) совпадение положительных результатов серологического анализа и клинического диагноза обнаружено в 97,2% случаев; у пяти больных данные серологического исследования были подтверждены гистологическим методом (в препаратах биоптатов антрального отдела и тела желудка, окрашенных по Гимза), цитологическим методом (в мазках-отпечатках биоптатов, окрашенных по Гимза) и уреазным методом с применением Де-нол теста. Положительный результат серологического теста у такого контингента больных является закономерным.
Параллельное определение чувствительности и специфичности препаратов фирм Орженикс и Био-Рад на 30 сыворотках обнаружило сходные результаты:
- чувствительность тест-системы ИммуноКомб фирмы Орженикс – 85 %,
- чувствительность тест-системы фирмы Био-Рад – 80%.
Если за точку отсчета брать данные, полученные при помощи референс-препарата Био-Рад, то чувствительность теста ИммуноКомб H.PILORI IGG составляет 100%, а специфичность – 71% (см.Таблицу 3) [40].
При сопоставимых характеристиках сравниваемых тестов в заключении ГИСКа им. Тарасевича [40] было отмечено, что тесты ИммуноКомб не требуют дополнительного оборудования, позволяют получать результат анализа через 66 минут и документировать его, делают доступным, наряду с групповым, индивидуальное тестирование. Наличие внутреннего контроля в тестах ИммуноКомб обеспечивает безошибочную постановку анализа и максимальную достоверность результата.
ИммуноКомб - оригинальная модификация Иммуноферментного анализа – единственные Иммуноферментные Быстрые Простые Тесты. В отличие от других БПТ и экспресс-тестов, чувствительность и специфичность ИммуноКомб достигает, а в некоторых случаях превосходит характеристики классических ИФА ELISA-тестов, требующих дорогостоящего оборудования, специальных помещений и подготовки персонала. Оснащение диагностической службы первичного медицинского звена БПТ ИммуноКомб H.PILORI IGG позволит своевременно и достоверно поставить диагноз и назначить адекватную медикаментозную терапию.
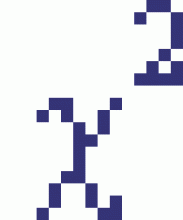
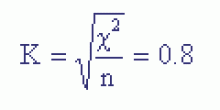

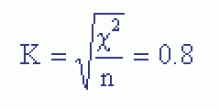
Оглавление
Чтобы просмотреть текст книги нажмите на нужную главу в оглавлении
Следующая часть
4.1.1. Количественное определение IgG к Н.Pylori иммуноферментным БПТ ИммуноКомб
Предыдущая часть
Глава 4. Описание медицинской технологии
Внешний вид