Наборы ИммуноКомб – простые быстрые тесты, предназначенные для диагностики СПИДА (ВИЧ1 и ВИЧ2), гепатитов A (HAV IgM, HAV Ab), B (HBsAg, anti-HBsAg, HBcIgG, HBcIgM), С (HCV), цитомегалии (CMV IgG, CMV IgM), токсоплазмоза (Toxo IgG, Toxo IgM), хламидиоза (Chlamidia Trachomatis IgG, Chlamidia Trachomatis IgM, Chlamidia Bivalent IgG), краснухи(Rubella IgG, Rubella IgM), гастритов и язвенных заболеваний (Helicobacter Pylori IgG). Типовой набор реагентов позволяет проводить анализ по единому плану, варьируя количество исследуемого образца, длительность и температуру инкубации в зависимости от специфичности набора. Для исследования используют сыворотку или плазму крови человека(в исключительных случаях цельную кровь). Такой унифицированный подход к диагностике различных инфекций намного упрощает подготовку персонала и работу в лаборатории в целом. Методика не требует наличия дополнительного оборудования. все компоненты набора готовы к употреблению. Набор рассчитан на 36 определений, включая два контроля, и может применяться для индивидуального тестирования образцов.
В этой главе приведено общее описание набора и схема постановки анализа. Методика анализа применительно к конкретной специфичности изложена в инструкции, прилагаемой к каждому набору ИммуноКомб, краткая инструкция представлена в таблице 32.
Таблица 32. Краткая инструкция и интерпретация результатов исследования с помощью теста ИммуноКомб
| Диагностика | Тест-системы ИммуноКомб | Время анализа, мин. | Разведение образца (мкл в мкл) |
Кол-во образца, мкл | t ,oC | Время инкубации в рядах ванночек, мин. | Резуль- тат |
Интерпретация положительной реакции | |||||
| A | B | C | D | E | F | ||||||||
| СПИДа | HIV 1+2 Bispot | 36 | НЕТ | 50 | 22-26 | 10 | 2 | 10 | 2 | 2 | 10 | да/нет | наличие антител ВИЧ 0,1,2 |
| HIV 1+2 CombFirm | 66 | НЕТ | 50 | 22-26 | 30 | 2 | 2 | 2 | 2 | 10 | да/нет | подтверждающий блот | |
| Гепатита А | HAV IgM | 184 | 10 в 490 | 25 | 37 | 120 | 2 | 30 | 20 | 2 | 10 | да/нет | активный гепатит А |
| HAV AB | 184 | 10 в 490 | 25 | 37 | 120 | 2 | 30 | 20 | 2 | 10 | да/нет | наличие HAV анитител | |
| Гепатита Б | HBs Ag'90 | 89 | 100 в 20 | 120 | 37 | 60 | 2 | 10 | 5 | 2 | 10 | да/нет | текущий гепатит B |
| HBc IgM | 96 | 10 в 490 | 25 | 22-26 | 60 | 2 | 20 | 2 | 2 | 10 | да/нет | активный гепатит B | |
| HBc IgG | 96 | 10 в 90 | 25 | 22-26 | 60 | 2 | 20 | 2 | 2 | 10 | да/нет | хронический гепатит с HBV | |
| Anti-HBs | 184 | НЕТ | 100 | 37 | 120 | 2 | 30 | 20 | 2 | 10 | ед/л | выздоровление/HBV иммунизация | |
| Гепатита С | HCV | 36 | НЕТ | 50 | 22-26 | 10 | 2 | 10 | 2 | 2 | 10 | да/нет | наличие HCV антител |
| Хламидиоза | Chl. trachomatis IgG | 46 | НЕТ | 10 | 22-26 | 10 | 2 | 20 | 2 | 2 | 10 | титр | хроническая инфекеция |
| Chl. trachomatis IgA | 76 | НЕТ | 25 | 22-26 | 40 | 2 | 20 | 2 | 2 | 10 | титр | активная и повторная инфекции | |
| Chl. Monovalent IgA | 96 | 25 в 75 | 25 | 37 | 60 | 2 | 20 | 2 | 2 | 10 | титр | активная и повторная инфекции | |
| Chl. Bivalent IgG | 106 | 10 в 310 | 20 | 22-26 | 60 | 2 | 30 | 2 | 2 | 10 | титр | хрон. Хл. трахоматис, пневмония | |
| Цитомегалии | CMV IgM* | 66 | 25 в 100 | 25 | 22-26 | 30 | 2 | 20 | 2 | 2 | 10 | да/нет | острая CMV инфекция |
| CMV IgG | 66 | 10 в 100 | 25 | 22-26 | 30 | 2 | 20 | 2 | 2 | 10 | ед/мл | хроническая CMV инфекция | |
| Краснухи | Rubella IgM* | 66 | 25 в 100 | 25 | 37 | 30 | 2 | 20 | 2 | 2 | 10 | да/нет | острая Rubella инфекция |
| Rubella IgG | 66 | 10 в 100 | 25 | 22-26 | 30 | 2 | 20 | 2 | 2 | 10 | ед/мл | хроническая Rubella инфекция | |
| Токсоплазмоза | Toxo IgM* | 56 | 10 в 100 | 25 | 22-26 | 20 | 2 | 20 | 2 | 2 | 10 | да/нет | острая Toxo ифнекция |
| Toxo IgG | 46 | НЕТ | 10 | 22-26 | 10 | 2 | 20 | 2 | 2 | 10 | ед/мл | хроническая Toxo инфекция | |
| Гастритов | H. pylori IgG | 66 | 10 в 100 | 25 | 22-26 | 30 | 2 | 20 | 2 | 2 | 10 | ед/мл | хроническая H. pylori инфекция |
Краткое описание процедуры анализа:
- Внести образцы и контроли в ряд А ванночек.
- Вставить гребень в ряд А. Инкубировать (время инкубации соответственно таблице).
- Повторить шаг 2 для рядов В, С, D, E, F.
- Вновь вставьте гребень в ряд Е на 1 мин.
- Результаты анализа появляются в виде окрашенных точек на зубцах гребня.
*Предварительно инкубировать образец в ряду А, затем вставить гребень.
Тесты ИммуноКомб постоянно модернизируются, чтобы соответствовать всем требованиям современной диагностики. Концепция ИммуноКомб учитывает особенность появления первых антител, которые отличаются от антител, полученных позднее, во время задержанного иммунного ответа: различные изотипы синтезированных антител, различную аффинность и авидность, направленность на различные эпитопы или различные антигены. Тесты сконструированы на основе высокоочищенных видоспецифических антигенов. Это позволяет избежать перекрестных реакций при обнаружении антител к соответствующему возбудителю и выявить возбудителя на ранней стадии заболевания.
Принцип анализа.
В наборах ИммуноКомб реализован принцип твердофазного иммуноферментного анализа (ИФА) в различных его вариантах. Например, для обнаружения антител к ВИЧ 1+2 и вирусу гепатита С применен непрямой метод ИФА, а для выявления HBsAg – "сэндвич" вариант.
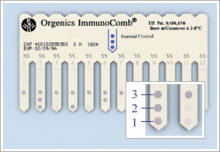
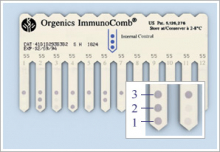
Рисунок 1. Гребень.
В качестве Твердой фазы использован пластиковый гребень с 12 зубцами, которые можно легко разделить при необходимости проведения индивидуального тестирования (рис.1). Нижняя часть каждого зубца в 2-3 точках сенсибилизирована специфическими антителами или антигенами в соответствии с назначением набора. Так, на гребне для обнаружения антител к ВИЧ1 и ВИЧ2 в нижней точке зубца сорбированны синтетические пептиды – производные env gp41 и gp120, характерные для ВИЧ1; в средней точке – синтетические пептиды – производные env gp36, соответствующие ВИЧ2; в верхней точке (внутренний контроль) – козьи антитела к иммуноглобулинам человека. Зубец гребня для обнаружения антител к вирусу гепатита С также сенсибилизирован в трех точках: нижнее – неструктурными антигенами HCV NS3, NS4, NS5; средняя – core антигеном HCV; верхняя(внутренний контроль) – иммуноглобулином человека. Зубец гребня для обнаружения поверхностного антигена вируса гепатита В (HBsAg) имеет две ативные точки: нижняя – моноклональные антитела к HBsAg; верхняя (внутренний контроль) – биотинимированный бычий сывороточный альбумин. И так далее в соответствии со специфичностью набора
Верхняя точка на каждом зубце является контрольной (внутренний контроль) и активирована таким образом, что в результате корректного проведения процедуры анализа обязательно приобретает окраску, подтверждая его достоверность. Нижняя и/или средняя точки окрашиваются при наличии в исследуемом образце искомых антител(АТ) или антигенов(АГ). Таким образом, при проведении анализа иммунное взаимодействие осуществляется на поверхности зубцов пластикового гребня, помещенного в специальную проявочную ванну .
Рисунок 2. Проявочная ванна.
Проявочная ванна (Рис. 2) имеет 6 рядов (A - F) по 12 лунок в каждом ряду. В лунках каждого ряда содержатся растворы веществ, готовые к употреблению на различных этапах проведения исследования. Анализ проводят шаг за шагом, перемещая гребень из одного ряда в другой и, инкубируя его на каждом этапе (Рис. 3). В начале анализа образцы исследуемой сыворотки или плазмы смешивают с раствором для разведения в лунках ряда А проявочной ванны. Затем в лунки ряда А опускают гребень. Искомые АТ или АГ, если они есть в исследуемой сыворотке (плазме), избирательно свяжутся со специфическими реагентами, фиксированными в средней и/или нижней точке зубца. Одновременно пойдет реакция образования иммунного комплекса в верхней точке зубца (внутренний контроль). Несвязавшиеся компоненты смывают в лунках ряда В. В лунках ряда С специфически связавшиеся компоненты опять будут реагировать с ферментным конъюгатом, содержащим щелочную фосфатазу. В следующих рядах ячеек несвязавшиеся компоненты опять удаляют промывкой. В лунках ряда F связанная (на зубце) щелочная фосфатаза взаимодействует с хромогенными компонентами. Результаты реакции наблюдают в виде серо-голубых пятен на поверхности зубца гребня.
Достоверность результатов анализа, проводимого с помощью системы ИммуноКомб подтверждается тремя обязательными контролями: внутренний контроль (описан выше) – обязательное появление окрашенного верхнего пятна на каждом использованном зубце; положительный и отрицательный контроли, которые должны использоваться при анализе каждой группы исследуемых образцов.
Положительный контроль – разведенная инактивированная человеческая плазма, содержащая минимальное диагностически значимое количество искомых антител или антигенов.
Отрицательный контроль – разведенная инактивированная человеческая плазма, несодержащая искомых антител или антигенов.
При проведении анализа положительный и отрицательный контроли тестируют параллельно с тестируемыми образцами и при оценке результатов сравнивают интенсивность окрашивания контрольных и анализируемых образцов. В результате тестирования, зубец гребня, взаимодействующий положительным контролем, должен иметь окрашенные верхнее, среднее и/или нижнее пятна; на зубце с отрицательным контролем должно появиться только верхнее пятно (внутренний контроль) и отсутствовать или иметь едва заметное окрашивание среднее и/или нижнее пятна. Верхнее пятно должно присутствовать на всех зубцах, задействованных при анализе. Несоответствие хотя бы одному из перечисленных трех требований свидетельствует о недостоверности полученных результатов(рис.4).
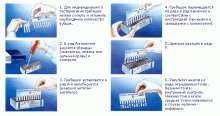
Схема постановки анализа
- Для индивидуального тестирования гребешок можно согнуть и отломить необходимое количество зубцов. В ванночке вскрывается соответствующее числу зубцов количество ячеек. Невскрытые ячейки и неиспользованные зубцы хранятся в течение срока годности тест-системы.
- В ряд А ванночки вносятся образцы (сыворотка, плазма или цельная кровь) и контроли.
- Гребешок вставляется в ряд А и инкубируется (реакция антиген-антитело).
- Гребешок перемещается из ряда в ряд ванночки в соответствии с инструкцией (промывки и связывание с коньюгатом).
- Цветная реакция в ряду F.
- Результат анализа в виде окрашенных точек.
Верхняя точка: внутренний контроль. Должна присутствовать и при положительных и при отрицательных образцах. Она подтверждает правильность работы тест-системы.
Нижняя точка (одна или две) появляется в случае наличия инфекции. Уровень видоспецифичных
антител в каждом образце оценивается количественно с помощью цветной шкалы КомбСкейл,
входящей в состав набора.
Рисунок 3. Схема постановки анализа
Состав набора
Гребни
Три пластиковых Гребня, по 12 зубцов, по зубцу на каждый тест. Каждый зубец сенсибилизирован в двух или трех точках:
- верхняя точка - внутренний контроль,
- средняя и/или нижняя точка - известные специфические реагенты - АГ или АТ (См. "Инструкцию", прилагаемую к конкретному набору). Гребни поставляются в алюминиевых упаковках, содержащих мешочек с влагопоглотителем.
Проявочные ванны
Три проявочные ванны, покрытые алюминиевой фольгой, состоящее из 6 рядов (A-F) по 12 лунок в каждом. Проявочная ванна (Рис.2) содержит все реагенты, необходимые для проведения анализа:
- ряд A-растворитель образца,
- ряд B-промывочный раствор,
- ряд C - специфические реагенты, меченые щелочной фосфатазой (конъюгат),
- ряд D - промывочный раствор,
- ряд E - промывочный раствор,
- ряд F - раствор хромогенного компонента, содержащий 5-бром-4-хлор-3-индозил фосфат (BCIP) и нитро синий тетразол (NTB)
Контроли
Положительный контроль - 1 флакон (красная крышка) - разбавленная инактивированная человеческая плазма, положительная по искомым АТ/АГ.
Отрицательный контроль - 1 флакон (зеленая крышка) - разбавленная инактивированная человеческая плазма, отрицательная по искомым АТ/АГ.
Разбавитель образца - 1 бутылочка (прозрачная крышка).Входит в состав набора в случае необходимости предварительной обработки образца.
Перфоратор - для прорывания алюминиевой фольги, покрывающей лунки Проявочной ванны.
Шкала CombScale® ?для считывания результатов анализа (только в наборах позволяющих получать количественную оценку результатов).
Методика анализа
Сбор образцов для анализа
В качестве исследуемых образцов используют сыворотку или плазму человека. Образцы хранят до 7 суток при температуре 2-8 oС. Для более длительного хранения образцы должны быть заморожены.
После оттаивания образцов отцентрифугируйте их. В анализ берите надосадочную жидкость. Избегайте повторных замораживаний и оттаиваний образцов.
Необходимое оборудование
- Шприц-пипетки со сменными наконечниками с объемами 10, 25 и 90 мкл.
- Лабораторный таймер или часы.
- Микропробирки или планшеты(для некоторых наименований).
Подготовка к анализу
Анализ проводится при комнатной температуре (22 – 26 oС).
Подготовка Проявочной Ванны
- 1.Выдержите Проявочную ванну в термостате при температуре 37 oС в течение 20 минут или оставьте при комнатной температуре в течение 3-х часов
- Застелите рабочий стол фильтровальной бумагой, которая после окончания работы должна быть уничтожена как биологически опасные отходы.
- Перемешайте реагенты, встряхивая Проявочную Ванну.
Примечание: Не удаляйте фольгу, покрывающую Проявочную Ванну. Вскрывайте фольгу только в соответствии с указаниями инструкции по проведению анализа с помощью сменного наконечника или перфоратора.
Подготовка гребня
Внимание. Чтобы обеспечить правильное функционирование теста, не прикасайтесь к зубцам гребня.
- Разорвите алюминиевую упаковку Гребня у надсеченного края. Извлеките Гребень.
- Вы можете использовать Гребень и Проявочную Ванну целиком либо использовать только часть Гребня и ячеек Проявочной Ванны. Чтобы использовать часть Гребня:
- Подсчитайте, сколько зубцов вам потребуется для анализа образцов и контролей. Вам потребуется по одному зубцу на анализ. На каждом зубце изображен кодовый номер анализа для того, чтобы всегда можно было определить к какому набору принадлежит отдельный зубец.
- Согните Гребня по вертикали и сломайте или отрежьте ножницами, чтобы отделить требуемое число зубцов (= число анализов + 2 контроля).
- Верните неиспользованную часть Гребенки в алюминиевую упаковку (вместе с мешочком влагопоглотителя). Плотно закройте упаковку, например, канцелярской скрепкой, чтобы избежать проникновения влаги. Храните Гребень в оригинальной коробке набора при температуре 2- 8 oС для дальнейшего использования.
Общая схема проведения анализа
Предварительное разведение образцов и контролей. (Требуется для некоторых наборов см. "Инструкцию", прилагаемую к набору).
-
Реакция Антиген - Антитело (Ряд А).
Наберите в пипетку разведенный образец в количестве, указанном в " Инструкции", прилагаемой к набору (от 10 до 50 мкл в зависимости от набора, см. табл.21). Проколите наконечником пипетки или перфоратором покрытие из фольги над одной из ячеек ряда А Проявочной Ванны и введите образец на дно ячейки. Перемешайте, многократно всасывая и вновь вводя раствор. Снимите наконечник пипетки.
- Повторите шаг 1 для других разведенных образцов и двух разбавленных контролей. Используйте новую ячейку из ряда А для каждого образца и контроля. Меняйте наконечник пипетки для каждого образца.
- Вставьте Гребень (стороной с надписями к себе) в ячейки ряда А, содержащие образцы и контроли. Перемешайте: выньте и вставьте Гребень в ячейки несколько раз.
- Оставьте Гребень в ячейках ряда А и выдержите в течение времени, указанного в "инструкции", прилагаемой к набору. Включите таймер. Перед окончанием экспозиции проколите перфоратором фольгу ячеек ряда В. Не открывайте большего, чем необходимо, числа ячеек.
- По истечении времени экспозиции выньте Гребень из ячеек ряда А.Удалите капли жидкости с заостренных концов Гребня с помощью чистой фильтровальной бумаги. Не прикасайтесь к фронтальной поверхности Гребня.
-
Первая промывка (ряд В).
Вставьте Гребень в ячейки ряда В. Прополощите: резко вынимайте и вставляйте Гребень в ячейки в течение, по крайней мере, 10 секунд, чтобы хорошо промыть его. Повторите полоскание несколько раз в течение 2 минут; в интервалах проколите фольгу ячеек ряда С. По истечении 2 минут выньте Гребень и удалите капли жидкости также, как на шаге 3c.
-
Связывание с Конъюгатом (ряд С).
Вставьте Гребень в ячейки ряда С. Перемешайте также как на шаге 3a. Включите таймер на время, указанное в "Инструкции", прилагаемой к набору. Проколите фольгу ячеек ряда D. После экспозиции выньте Гребень и удалите капли жидкости.
-
Вторая промывка (ряд D).
Вставьте Гребень в ячейки ряда D. В течение 2 минут несколько раз прополощите также как на шаге 4. Проколите фольгу ячеек ряда Е.По истечении 2 минут выньте Гребень и удалите капли жидкости.
-
Третья промывка (ряд Е).
Вставьте Гребень в ячейки ряда Е. Несколько раз прополощите в течение 2 минут. Проколите фольгу ячеек ряда F. По истечении 2 минут выньте Гребень и удалите капли жидкости.
-
Цветная реакция (ряд F).
Вставьте Гребень в ячейки ряда F .Перемешайте. Включите таймер на 10 минут. Через 10 минут выньте Гребень.
-
Остановка реакции (ряд Е).
Вставьте Гребень снова в ячейки ряда Е. По истечении 1 минуты выньте Гребень и дайте ему высохнуть на воздухе.
Удаление отходов.
Использованные Проявочные Ванны, наконечники пипеток, фильтровальная бумага должны уничтожаться как биологически опасные отходы. Использованные перчатки обрабатываются замачиванием в дезрастворах (например, в 3-6 %-ном растворе перекиси водорода).
Хранение неиспользованных частей набора
Если Вы использовали не все ячейки Проявочной Ванны, Вы можете сохранить ее для дальнейшего использования: заклейте использованные ячейки широкой клейкой лентой так, чтобы ничего не могло вылиться из ячеек даже, если Проявочная Ванна будет перевернута. Верните оставшиеся Проявочные Ванны, Гребни, перфоратор, контроли, разбавители образцов и "Инструкцию" в оригинальную коробку. Храните в бытовом холодильнике при температуре 2–8 oС.
Результаты анализа
Достоверность анализа
В набор входит "положительный контроль" и "отрицательный контроль", которые должны использоваться при анализе каждой группы исследуемых сывороток (плазмы). На зубце с положительным контролем должны быть два (или три) пятна: верхнее - внутренний контроль, среднее и/или нижнее - специфический положительный контроль (Рис.5). На зубце с отрицательным контролем появится только верхнее пятно (внутренний положительный контроль), а среднего и/или нижнего пятна вовсе не должно быть либо оно будет очень слабым (еле заметным). Верхнее пятно также должно появиться на всех остальных (опытных) зубцах, тем самым подтверждая, что набор работает правильно.
Рисунок 5. Достоверность результатов
Качественная оценка результатов
Для визуальной оценки результатов анализа следует сравнить интенсивность окрашивания нижнего пятна каждого образца с интенсивностью окрашивания нижнего пятна на зубце с положительным контролем. Пятно с интенсивностью окрашивания большей или равной интенсивности окраски пятна положительного контроля указывает на наличие антител к возбудителю в исследуемом образце.
Отсутствие пятна или пятно с интенсивностью окрашивания меньшей, чем положительный контроль указывает на отсутствие антител к возбудителю в исследуемом образце.
Количественная оценка результатов
Количественная оценка результатов осуществляется с помощью шкалы CombScale, прилагаемой к набору Иммунокомб (Рис. 7).
Откалибруйте CombScale. Поместите нижнюю точку Положительного Контроля под участком шкалы с наиболее близкой окраской. Сдвиньте линейку так, чтобы надпись "C+" появилась в окошечке над участком шкалы с выбранной интенсивностью окраски.
Считайте результаты не меняя калибровочного положения линейки. Для каждого образца подберите участок шкалы, наиболее близкий по интенсивности окраски к окраске нижней точки на зубце. Запишите концентрацию (в Ед./мл) по числу в окошке над этим участком как приблизительный титр антител соответствующего образца.
Рисунок 7. Шкала CombScale™
Автоматизированная оценка и интерпретация результатов
Результаты анализа можно учитывать автоматически, на приборе Комбскан III™(CombScan III™), производства фирмы Орженикс. Система Комбскан III™ использует принципиально новую функцию для обработки оптической плотности точек на сканируемых диагностических Гребнях, позволяющую количественно оценивать титр антител в крови.
Данный прибор совместим со всеми существующими операционными системами, предназначенными для ПК производства корпорации Microsoft. Прибор Комбскан III™ адаптирован для российских пользователей. Хранит архив данных и позволяет выводить данные на экран и принтер. Надежная система проверки позволяет избежать дублирования данных. Графический интерфейс разработан специалистами в области компьютерного дизайна и производства диагностических приборов. Позволяет создать систему пользователей с различными степенями допуска. Обладает легкой системой поиска в базе данных.
Для работы со сканером CombScan III™ необходимы: персональный компьютер ПЕНТИУМ с присоединением универсальной последовательной шины USB и операционные системы(Microsoft Windows ’98 или Microsoft Windows Millennium, или Microsoft Windows 2000, или Microsoft Windows XP. Установите программное обеспечение сканера до подключения сканера к Вашему компьютеру. Выполните валидацию сканера (проверку его работоспособности) перед сканированием гребня. Для валидации вашего сканера CombScan III™ пользуйтесь исключительно гребенем для подтверждения‚ поставляемым с программой CombScan III™.
Установите Гребень в смотровую рамку лицевой стороной к стеклу (Рис. 8). Выровняйте прямую часть гребня с краем смотровой рамки. При этом зубцы гребня должны быть направлены к центру окна.
Рисунок 8. Установка гребня в сканере
Как только CombScan III™ прошел стадию валидации, он готов к сканированию и анализу гребня. Тест должен включать, по меньшей мере, один позитивный контроль‚ чтобы CombScan III™ мог его прочитать и интерпретировать.
При использовании части гребня укажите число зубцов. Обратите внимание‚ что номера зубцов‚ которые не прочитаны‚ окрашиваются в розовый цвет (т е. они бездействуют). После введения всех данных гребня установите его лицевой стороной к считывающей стеклянной рамке на сканере.
После успешного сканирования появится экран результатов. Зеленый прямоугольник в левом верхнем углу экрана указывает на то‚ что сканер был успешно аттестован. Красный прямоугольник говорит о том‚ что сканер не аттестован. Это состояние закрывает доступ к клиническим данным. Вы можете увидеть клинические данные‚ значения абсолютной и удельной поглощающей способности‚ щелкнув соответствующие клавиши в левой нижней части экрана. Дополнительно к значениям поглощающей способности‚ экран показывает клинические данные исследования‚ окрашенные согласно приведенной ниже таблице 4.
Таблица 4. Клинические данные исследования
| Цвет записи | Значение |
| Черный | Прошел положительную или отрицательную проверку |
| Розовый | Не прошел положительную или отрицательную проверку |
| Красный | Положительный результат |
| Зеленый | Отрицательный результат |
| Коричневый | Недействительный результат |
Результаты исследования сохраняются автоматически в виде файла. Для получения распечатки результатов щелкните «печать».
Документация результатов
В связи с тем, что окраска точек является стабильной, гребень следует хранить для дальнейшей документации.
Ограничения
Результаты анализа с помощью наборов ИммуноКомб, как и результаты любых других анализов, предназначенных для диагностики in vitro , следует оценивать с учетом клинического обследования пациентов.
Меры предосторожности
- Наборы Иммунокомб можно использовать только для in vitro диагностики.
- Человеческие материалы, использованные при изготовлении набора, были проверены на инфекционную безопасность и проявили отрицательную реакцию на HBsAg , на антитела против вируса гепатита С и на антитела к ВИЧ. Но так как никакой анализ не может дать полной гарантии отсутствия инфекционных контаминантов, со всеми контрольными растворами и человеческими образцами следует обращаться как с потенциально опасными.
- Работа должна проводиться в хирургических перчатках и лабораторной одежде. Выполняйте принятые в Вашей лаборатории правила техники безопасности.
- Не засасывайте растворы в пипетки ртом.
- Обращайтесь со всеми образцами, использованными Гребнями, Проявочными Ваннами и другими материалами набора как с потенциально опасными отходами.
- Не смешивайте реагенты разных наборов.
- Не используйте наборы с истекшим сроком хранения.
Хранение наборов ИммуноКомб
Храните наборы в оригинальной упаковке, при температуре 2-8oС. При этих условиях набор остается стабильным до срока, указанного на этикетке. Не замораживайте набор.













Оглавление
Чтобы просмотреть текст книги нажмите на нужную главу в оглавлении
Следующая часть
Глава XII. Подтверждающие тесты
Предыдущая часть
Глава X. Использование быстрых простых тестов для диагностики ВИЧ рожениц с неизвестным ВИЧ-статусом
Внешний вид