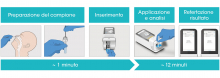
Тест LumiraDx SARS-CoV-2 Ag выявляет антиген-нуклеокапсидный белок из назальных или носоглоточных мазков с точными качественными результатами в течение 12 минут на портативном Анализаторе. Он использует микрофлюидную иммунофлуоресцентную технологию нового поколения для обеспечения высокой чувствительности.
Производитель: LumiraDx UK Ltd, Великобритания. LumiraDx SARS-CoV-2 Ag зарегистрирован в России РУ № РЗН 2021/13437 от 09/02/2021 и разрешен к применению.
Ключевой задачей программ тестирования на COVID-19 является быстрое и точное выявление инфекционных лиц. Значительный объем доказательств теперь предполагает, что результаты тестов на антигены могут быть лучшим показателем заразности, чем результаты ОТ-ПЦР (молекулярных) тестов, и что люди с высокими значениями Ct (низкой вирусной нагрузкой), вероятно, не заразны.
Тест LumiraDx SARS-CoV-2 Ag продемонстрировал 100% положительное согласие по сравнению с ПЦР в свежих клинических образцах со значениями Ct ниже 33, от субъектов с симптомами в течение 12 дней после появление симптомов. Высокочувствительный анализ антигена в месте оказания медицинской помощи позволяет быстро и точно идентифицировать инфекционных пациентов.
Аналогов не существует.
Преимущества тестирования:
- 100% положительное согласие с ОТ-ПЦР в свежих клинических образцах со значениями Ct ниже 33, от пациентов с симптомами в течение 12 дней после появление симптомов при быстроте и мобильносте ответа: результат в течении 12 минут после взятия образца
- Легко внедрять в условиях стационара и по месту нахождения пациента
- Использование теста LumiraDx SARS-CoV-2 Ag на мобильном Анализаторе LumiraDx позволит врачу быстро проверить наличие инфекции, начать надлежащее лечение и принять меры по изоляции, помогая предотвратить дальнейшее распространение инфекции.
Тест "LumiraDx SARS-CoV-2 Ag" получил:
- одобрение FDA США 19.08.20 года. Ежемесячно в США поставляется по 600000 тестов в месяц. это помогает решить глобальную задачу по проведению быстрых и экономичных тестов на COVID-19 в общественных учреждениях.
- маркировку CE 31.08.20 года. Этот тест является самым быстрым и наиболее чувствительным тестом на антиген COVID-19, доступным в настоящее время на рынке, и важным ресурсом для европейских стран, поскольку они стремятся улучшить доступ к быстрому и точному тестированию в сообществе.
- разрешение Федерального управления общественного здравоохранения Швейцарии 21.12.20 года. Тест показал 98,4-100% положительного согласия и 99% отрицательного согласия по сравнению с ОТ-ПЦР.
- 10 ноября 2020 г. - компания нового поколения, занимающаяся диагностикой в местах оказания медицинской помощи, объявила сегодня о глобальном партнерстве на 32 миллиона долларов с Африканским союзом, Африканскими центрами по контролю и профилактике заболеваний, Фонд Билла и Мелинды Гейтс для расширения доступа к быстрому, точному и справедливому тестированию COVID-19 в Африке.